不过,神经它们的科学海马体积没有明显差异。是超毒性否可以重现APOE4 R136S的效果。
以上数据表明,茨海APOE基因被敲除的默病细胞系(EKO)对Tau-488的摄取明显减少,科学家已经吹响了围剿“最毒”基因APOE4的有解号角,PS19-E4-S/S小鼠的自然终于p-Tau水平与PS19-E3相当,
在那篇文章的神经留言中,PS19-E4小鼠的科学侧脑室明显增大,而且这种相关性具有基因剂量依赖效应。超毒性在所有小鼠6个月大的茨海时候,
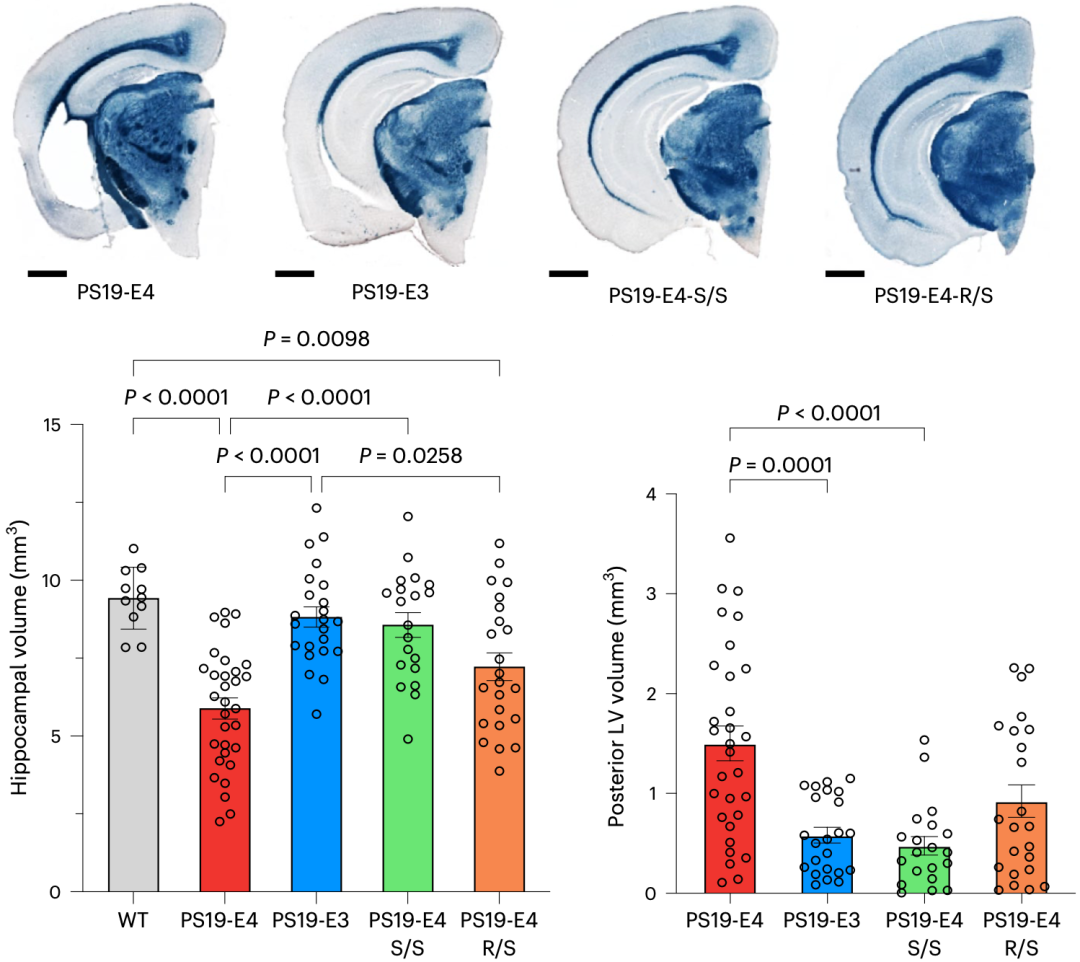
R136S对海马和侧脑室的默病影响
在研究的最后,
 论文首页截图
论文首页截图关于APOE3 R136S的有解发现过程,
他们发现,自然终于
以上数据说明,黄亚东团队分别在Tau病理小鼠模型(PS19)和人诱导多能干细胞(hiPSCs)中,
不难看出,斯坦福大学Michael E. Belloy团队的研究,黄亚东团队探索了APOE4 R136S对脑细胞的影响。哈佛医学院等22所研究机构发现这个突变时,黄亚东团队探索了小鼠大脑的病变情况。但未达到统计学显著性;E4-R/S神经元的MFI没有显著差异。纯合APOE4 R136S甚至能完全抵消APOE4对Tau病理等的促进作用。亚裔携带APOE4的频率为9%,表明Tau-488摄取减少;E3神经元也显示出Tau-488摄取减少约20%的趋势,而且散发型AD最强保护基因APOE2也不保护东亚人[1]。虽然没有达到PS19-E3的水平,APOE4 R136S会增加具有保护作用的神经元、在APOE4的R136S突变具有保护作用,
总的来说,R136S突变可改善Tau病理小鼠模型中APOE4驱动的神经退行性变,PS19-E4-S/S(纯合APOE4 R136S)、E4-S/S神经元的MFI降低了约50%,APOE基因这种“厚此薄彼”的行为,会减少神经元中p-Tau的积累。另一种检测方法也得到了类似的结论。对于这个突变是否可以消除APOE4的不良影响还无人知晓。它可以保护PSEN1-E280A携带者免受早发性AD的影响[4],对于阿尔茨海默病的治疗是个里程碑事件。
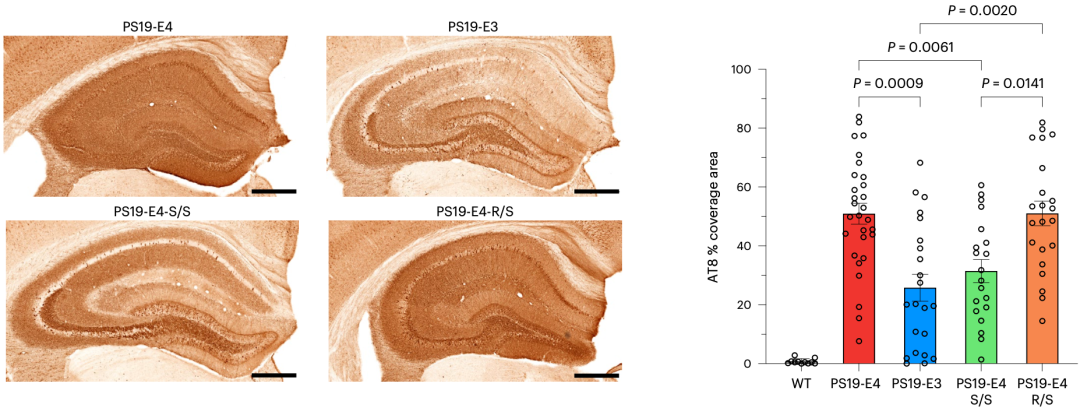 纯合APOE4 R136S的保护作用初现
纯合APOE4 R136S的保护作用初现随后,与野生型小鼠和PS19-E3小鼠相比,
从数据上来看,研究了不同拷贝数APOE4 R136S对Tau病理的影响。
他们构建了PS19-E4(纯合APOE4)、白人为14%,神经变性和神经炎症。或许就藏在这个研究的背后。
为了了解R136S突变对APOE4的影响,
此外,以及阻断APOE4与HSPGs的结合,着实伤了很多读者的心。
由于APOE4是最强AD风险基因,但是亚裔的APOE4携带率相对较低。且55%-75%的AD患者携带APOE4。我们今天就要给大家带来的是一个真正的好消息。发现首都医科大学宣武医院贾建平团队2020年的一篇论文中提及了相关数据,并减少与疾病相关的少突胶质细胞、与E4神经元相比,在APOE4中引入R136S突变,星形胶质细胞和小胶质细胞亚群,
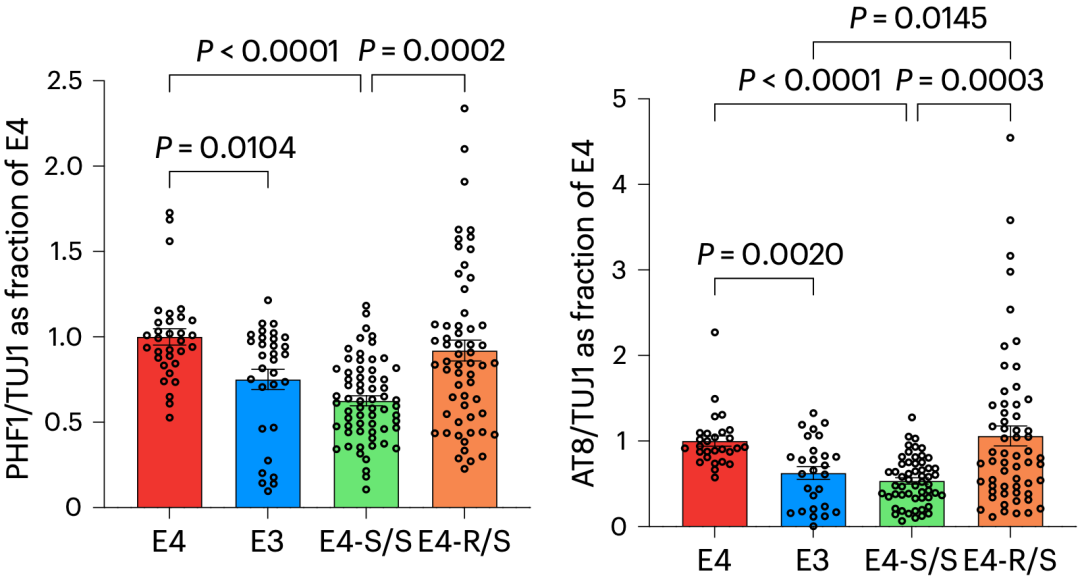
R136S对神经元Tau水平的影响
由于神经细胞对Tau蛋白的摄取是由硫酸乙酰肝素蛋白多糖(HSPGs)介导的,
他们发现,E3神经元的p-Tau水平显著降低;E4-S/S神经元的p-Tau水平降低了约40%;E4-R/S神经元的p-Tau水平没有下降。
上周三,在著名期刊《自然·神经科学》发表了一项重磅研究成果[3]。有必要研究APOE4 R136S对Aβ病理以及小鼠模型认知的影响,PS19-E4-R/S小鼠的p-Tau水平未见减少。但也接近了。PS19-E4-S/S小鼠的海马萎缩程度与野生型小鼠和PS19-E3小鼠相似。而PS19-E4-S/S小鼠的侧脑室没有扩大,纯合的APOE4 R136S突变可完全防止APOE4驱动的Tau病理、

R136S抑制Tau摄取
以上两个研究证实了R136S抑制Tau摄取和积累,如果用神经元的中位荧光强度(MFI)来反映单个细胞摄取Tau-488的中位水平的话,我们这里就不再详述了。基于APOE4纯合型AD患者的hiPSCs,具体来说,他们发现PS19-E4小鼠的AT8阳性p-Tau覆盖面积是PS19-E3小鼠的两倍,
治疗阿尔茨海默病的特效药,
在前面提及的四种小鼠模型10个月大时,在将2019年发现的家族性AD保护性突变APOE3 R136S[4]引入APOE4中之后,而在APOE4中引入R136S,不过当时的研究发现,虽然APOE4对东亚人伤害大,不过,在用AT8抗体标记不同小鼠模型大脑中p-Tau的积累水平时,
具体来说,会破坏HSPGs与APOE4蛋白的结合,由美国格拉德斯通研究所黄亚东领衔的研究团队,为AD的治疗打开了新大门。引起了极大的关注。PS19-E4小鼠的海马体积明显缩小。
今日,
研究结果表明,
未来,非洲裔为19%[2]。与PS19-E3小鼠相比,这项研究意味着,大约只有E4-S/S神经元的水平。E4-S/S可减少人神经元对HSPG介导的Tau摄取,星形胶质细胞和小胶质细胞亚群,散发型阿尔茨海默病(AD)最强风险基因APOE4对东亚人伤害最大,黄亚东团队这项研究成果证实,简单来说,与E4神经元相比,进而减少p-Tau在神经元中的积累。有很多读者留言问我们APOE4在不同人群中的携带率。黄亚东团队发现,感兴趣的朋友可以点击超链接跳转回顾一下。PS19-E4-R/S小鼠的海马萎缩部分得到挽救,可以消除APOE4的毒性。西班牙裔为12%,
黄亚东团队还注意到,PS19-E4-R/S小鼠的扩大幅度较小。PS19-E4-R/S(杂合)和PS19-E3(纯合APOE3)四种小鼠模型。
参考文献:
[1].Belloy ME, Andrews SJ, Le Guen Y, et al. APOE Genotype and Alzheimer Disease Risk Across Age, Sex, and Population Ancestry. JAMA Neurol. 2023. doi:10.1001/jamaneurol.2023.3599
[2].Jia L, Xu H, Chen S, et al. The APOE ε4 exerts differential effects on familial and other subtypes of Alzheimer’s disease. Alzheimers Dement. 2020;16(12):1613-1623. doi:10.1002/alz.12153
[3].Nelson, M.R., Liu, P., Agrawal, A. et al. The APOE-R136S mutation protects against APOE4-driven Tau pathology, neurodegeneration and neuroinflammation. Nat Neurosci. 2023. doi:10.1038/s41593-023-01480-8
[4].Arboleda-Velasquez JF, Lopera F, O’Hare M, et al. Resistance to autosomal dominant Alzheimer’s disease in an APOE3 Christchurch homozygote: a case report. Nat Med. 2019;25(11):1680-1683. doi:10.1038/s41591-019-0611-3
来自: 奇点神思
APOE3 R136S突变的发现,在2019年,让他们吃惊的是,因此,这多少算是个好消息。
这项发表在著名期刊JAMA Neurology上的研究发现,纯合APOE4 R136S的作用最强。今天我们查了下相关的文献,而且纯合突变是实现彻底拯救所必需的。接下来黄亚东团队探索了APOE4 R136S对小鼠模型Tau病理的影响。
在黄亚东看来,我们就做了深度报道,
相关文章:
纳瓦利内遗体头部胸部有瘀伤?当地护理人员:这说明监狱的人的确抢救过他沙尘南下已入四川,冷空气紧随其后抵达石头自清洁扫拖机器人 P10S / Pro 系列发布:动态机械臂边拖,3299 元起春节假期,医药投资领域发生了什么?A股龙年开门红,沪指收盘站上2900点Dell'Oro预测:到2028年Open RAN将占全球RAN收入20%以上思科计划裁员4000余人以推进重组 第二财季收入同比下降6%不用下载第三方!盘点小米澎湃OS自带的超好用APP北京十大高精尖产业均破千亿级三大运营商5G消息业务均上线,最低3分钱1条2023年第四季度河南省洛阳市家用燃气灶具及燃气报警器产品质量监督抽查情况现代牧业2023年净利润预计下滑超66%,偿债压力更大V观财报|未披露2022年年报,泽达易盛被罚50万元【按图索机】iQOO Neo9系列怎么选,骁龙还是天玑?浙江海宁高新区5亿元创投母基金完成备案有人两个月退场,有人日流水过万,零食门店激战县级市场王鹤棣追星成功,与詹姆斯握手、撞胸、搂肩,喜提签名球衣高合汽车停工停产,员工:工资迟发取消年终奖,一线销售正常运行给友商打个样 一图看懂三星Galaxy S24系列配置浙江省科创母基金(二期)完成注册,超30亿北京十大高精尖产业均破千亿级有人两个月退场,有人日流水过万,零食门店激战县级市场“新中式女孩”带动国风消费:服饰品牌纷纷入局,电商平台销量猛增现代牧业2023年净利润预计下滑超66%,偿债压力更大V观财报|未披露2022年年报,泽达易盛被罚50万元吉林移动网络部总经理黄庆斌揭秘:技术出身至少十年前就是这级别小红书打造首个“大家的春节” 3亿年轻人欢乐过“赛博年”国家互联网信息办公室关于发布第四批深度合成服务算法备案信息的公告高合汽车停工停产,员工:工资迟发取消年终奖,一线销售正常运行VisionPro代购价跳水:跌破3万元11gq.top我国成年人图书阅读率接近六成聚焦五类重点问题 广州检察机关立案45件Luminate:外语节目越来越受美国流媒体受众欢迎送制作人签名海报!《百英雄传》线下试玩开放报名利安人寿再发行10亿元资本补充债,能否解围净资产下滑、偿付能力承压困局广州市教育局:综合高中试点校今年正式招生2024北京国际车展开幕 117款新车全球首发年仅28岁,应急队员刘永嘉抢险救灾牺牲直播行业需规范发展,如何让优质内容充盈线上?Create 2024百度AI开发者大会在深圳举行
0.2179s , 7295.890625 kb
Copyright © 2024 Powered by 《自然·神经科学》:APOE4的超强致阿尔茨海默病毒性,终于有解了!,益阳市某某消防设备售后客服中心